Choque de partículas:
Tudo o que vemos e tocamos possuem uma origem e são constituídos sistematicamente por átomos, que são constituídos essencialmente por prótons, nêutrons e elétrons. Todos os elementos químicos, como eu descrevi, são do processo de fusão nuclear, ou seja, choque de prótons com outras partículas presente na quele ambiente de altíssima pressão e temperatura, devido a gravidade que tenta comprimir o gás e a poeira cósmica em um lugar de aglutinação de matéria (nebulosa, glóbulo molecular, próton-estrela e a estrela definitiva).
Exemplo de fusão nuclear, sendo o processo de transmutação do hidrogênio(H) em hélio(He), dois próton de cor vermelha e dois nêutron de cor amarela.
O choque dessas partículas formam o núcleo da estrela jovem e percorre até a fase que a gravidade vence com sua grande compressão. A compressão imensa que a gravidade exerce sobre a estrela é essencial, com a grande pressão e temperatura geradas na compressão do gás e poeira, que resulta na velocidade de movimento em direções diferentes das partículas, elas consequentemente se chocam no núcleo. Vimos esse processo ocorre com os diversos tipos de isotopos do hidrogênio, gerando os elementos químicos inicias da tabela periódica, ou seja, de acordo com seu número atômicos: 1H (hidrogênio), 2He (hélio), 3Li (lítio), 4Be (berílio), 5B (boro), 6C (carbono), 7N (nitrogênio), 8O (oxigênio), e outros elementos químicos de acordo com a complexidade do número atômico, formando camas na estrela.
A larga escala de produção de matéria no núcleo, acaba gerando camas de elementos químicos, os mais leves ficam nas camadas superiores e os com maior número atômico ficam no núcleo (nas camadas acima dele e no próprio núcleo).
O processo de síntese dos diversos tipos de átomos que utilizam os isótopos de hidrogênio (prótio, deutério e trítio) denomina-se: Cadeia próton-próton(Ciclo de próton-próton) e o processo de nome ciclo CNO(Ciclo carbono-nitrogênio-oxigênio).
Cadeia próton-próton ou ciclo próton-próton:
Processo da junção de hidrogênio(prótio, deutério e trítio) em hélio(4He, dois prótons + dois nêutrons) que liberar energia para manter a estrela contra a imensa compressão da gravidade. Esse fenômeno é natural e ocorre em todas as estrelas, porém este processo é extremamente comum nas estrelas do tipo do sol ou menores.
Modelo simplificado de um isótopo de prótio
O processo conduz na união de dois núcleos de hidrogênio 1H(prótio) a 2H(deutério), esse fenômeno libera um pósitron e um neutrino ao transformar um próton em um nêutron, a reação:
1H + 1H → 2H + e- + Ve(neutrino)
O deutério produzido na reação anterior pode se fusionar com outro núcleo de hidrogênio para formar um isótopo leve de hélio (3He).
2H + 1H → 3He + γ + 5.49 MeV
O neutrino liberado nesta reação, portam energias acima dos 0,42 MeV (Mega elétron volt). O pósitron resultante desse processo é anulado com o choque com um elétron e a massa se converte em energia na liberação de dois raio gama, veja a equação:
e+ + e- → 2γ + 1.02 MeV
A cadeia próton-próton é dividida em quatro denominações:
Cadeia próton-próton I ou cadeia pp I: Esse processo pp I ocorre com grande frequência de 91% na cadeia de fusão dos prótons e nêutrons, e a implicação no balanço final de 26,7 MeV. Essa cadeia é dominante a temperaturas de 10 a 14 megakelvin(MK), com temperaturas abaixo de 10MK ocorre a pouca produção de 4He é baixa.
3He + 3He → 4He + 1H + 1H + 12.86 MeV
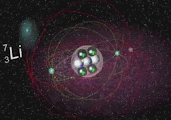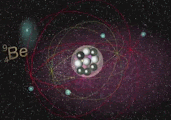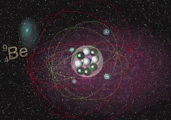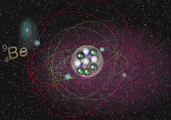
Cadeia próton-próton II ou cadeia pp II: Este processo requer maior temperatura, sendo de 14 a 23 Megakelven(MK). A produção de neutrinos nesta reações do Berílio e o Lítio 7Be(e-, Ve)7Li, liberando uma energia de 0,861 MeV, o restante emitindo 0,383 MeV.
3He + 4He → 7Be + γ
7Be + e- → 7Li + Ve
7Li + 1H → 4He + 4He
Cadeia próton-próton III ou cadeia pp III: o fenômeno ocorre sobre a temperatura de 23 MK, com a força cinética dos átomos sobre a grande temperatura original os isótopos de Berílio (7Be, 4 prótons e 3 nêutrons) e Boro(8B, 5 prótons e 3 nêutrons), esse isótopos são instáveis e consequentemente entram em estado de decaimento do par de prótons.
Cadeia próton-próton I ou cadeia pp I: Esse processo pp I ocorre com grande frequência de 91% na cadeia de fusão dos prótons e nêutrons, e a implicação no balanço final de 26,7 MeV. Essa cadeia é dominante a temperaturas de 10 a 14 megakelvin(MK), com temperaturas abaixo de 10MK ocorre a pouca produção de 4He é baixa.
3He + 3He → 4He + 1H + 1H + 12.86 MeV
Cadeia próton-próton II ou cadeia pp II: Este processo requer maior temperatura, sendo de 14 a 23 Megakelven(MK). A produção de neutrinos nesta reações do Berílio e o Lítio 7Be(e-, Ve)7Li, liberando uma energia de 0,861 MeV, o restante emitindo 0,383 MeV.
3He + 4He → 7Be + γ
7Be + e- → 7Li + Ve
7Li + 1H → 4He + 4He
Átomo de Lítio(Li) e Berílio(Be), e seus respectivos elétrons.
Cadeia próton-próton III ou cadeia pp III: o fenômeno ocorre sobre a temperatura de 23 MK, com a força cinética dos átomos sobre a grande temperatura original os isótopos de Berílio (7Be, 4 prótons e 3 nêutrons) e Boro(8B, 5 prótons e 3 nêutrons), esse isótopos são instáveis e consequentemente entram em estado de decaimento do par de prótons.
3He + 4He → 7Be + γ
7Be + 1H → 8B + γ
8B → 8Be + e+ + Ve
8Be ↔ 4He + 4He
Cadeia próton-próton IV(pp IV) ou Hep(hélio-próton): o isótopo de hélio-3(3He) reage com um prótio para formar o isótopo de hélio-4(4He). No processo de reação do hélio-3 para formar hélio-4 ocorre a perda de massa dos prótons, essa massa se converte em energia (raios gama) e neutrinos liberados nas reações individuais. A quantificação desta cadeia hélio-próton é de 26,73 MeV.
Reação próton-elétron-próton (pep): fenômeno raro, porém ocorre junto com o ciclo próton-próton. Essa reação trata-se do choque de três partículas simultaneamente, tendo um grande grau de improbabilidade de ocorre no núcleo da estrela.
A energia liberada pelos neutrinos nesta reação equivalem a 1,44 MeV, sendo mais energético do que a ciclos pp com 0,42 MeV.
3He + 1H
Reação próton-elétron-próton (pep): fenômeno raro, porém ocorre junto com o ciclo próton-próton. Essa reação trata-se do choque de três partículas simultaneamente, tendo um grande grau de improbabilidade de ocorre no núcleo da estrela.
1H + e- + 1H
A energia liberada pelos neutrinos nesta reação equivalem a 1,44 MeV, sendo mais energético do que a ciclos pp com 0,42 MeV.
Ciclo Carbono-Nitrogênio-Oxigênio
O ciclo carbono-nitrogênio-oxigênio é o segundo processo da reações nucleares nas estrelas, sob temperaturas superiores a do ciclo próton-próton. O ciclo próton-próton é importante para todas as estrelas, como o Sol e outras estrelas com massa igual ou menor. A cadeia próton-próton é substituído pela cadeia CNO, ocorre em estrelas massivas, já que este processo é semelhante ao próton-próton que origina núcleos atômicos com maior conjunto de partículas sub-atômicas unidas.
Como o ciclo pp, o ciclo CNO é dividido em CNO-I, CNO-II e Ciclo OF.
CNO-I: primeiro ciclo da reação, o carbono(C) inicial da reação é retorna com um núcleo de hélio(He).
12C + 1H
13N → 13C + e+ + Ve
+ 1,37 MeV
13C + 1H → 14N + γ + 7,54 MeV
14N + 1H → 15O + γ + 7,35 MeV
15O → 15N + e+ + Ve
+ 1,86 MeV
15N + 1H → 12C + 4He
+ 4,96 MeV
CNO-II: esse fenômeno ocorre com baixíssima frequência na estrela, onde o produto final é o 16O (isótopo de oxigênio) e um fóton, veja as equações:
O Ciclo CNO-I e suas reações.
CNO-II: esse fenômeno ocorre com baixíssima frequência na estrela, onde o produto final é o 16O (isótopo de oxigênio) e um fóton, veja as equações:
15N + 1H → 16O + γ + 12.13 MeV
16O + 1H → 17F + γ + 0.60 MeV
17F → 17O + e+ + Ve
+ 2.76 MeV
17O + 1H → 14N + 4He
+ 1.19 MeV
14N + 1H → 15O + γ + 7.65 MeV
15O → 15N + e+ + Ve
+ 2,75 MeV
As reações do nitrogênio(N) e a do oxigênio(O) ocasiona um núcleo de flúor(F) que está estável, sendo catalítico e não se acumula no núcleo da estrela.
Ciclo OF: processo que ocorre em estrelas com grande quantidade de massa. Na ação do ciclo CNO-II existe a produção do isótopo de flúor-18 (18F) e raios gama(γ) ao invés de um núcleo de nitrogênio(14N) e partículas alfa (α).
15N + 1H → 16O + γ
16O + 1H → 17F + γ
17F → 17O + e+ + Ve
17O + 1H → 14N + 4He
O resultado líquido de todos os ciclo CNO sempre são os mesmo:
4 p → 4He + 2 e+ + 2 Ve +
26.38 MeV